天然産物在藥物發現中具有重要作用。大部分天然藥物經過長期的臨床應用,療效确切,使用安全性高。目前有60%的臨床應用藥物來自天然産物及其衍生物。因此,從天然産物中尋找高效低毒易得的先導化合物是藥物研究的熱點。而曆史悠長的中藥大部分雖沒有明确的分子靶點和清晰的作用機制,但一些基于中藥來源的天然小分子化合物在抗腫瘤研究中已展示出獨特優勢,如改善症狀、減少複發與轉移、延長生存期,亦或增加化療藥物敏感性、減少毒副作用等。因此,仍有大量的天然産物等待人們去挖掘,是否存在抗腫瘤的特效小分子藥物也需要進一步研究。然而,活性小分子篩選的大體量性和活性小分子藥物的非特異性毒性給其疾病治療應用帶來瓶頸。為突破這一局限性,劉斌教授團隊從中藥蟾酥和植物大麻篩選活性小分子,以這些天然活性小分子藥物為基礎,探索可增強其藥效及安全性的構建策略,在2023年發展了系列抗腫瘤藥物。
1)發現大麻來源的活性小分子CBD調控TNBC細胞的自噬進程。基于CBD和CO供體構建了仿生CBD協同CO納米制劑,利用CBD對Nrf2的調控放大CO對線粒體的氧化應激刺激。其次,納米制劑通過調控ROS/JNK/Beclin1通路和下調LAMP1增強自噬小體的積累和破壞自噬溶酶體的形成,最終導緻細胞過度自噬而改善TNBC治療。相關工作于2023年5月發表于Acta Pharmaceutica Sinica B雜志,論文第一作者為博士生肖暢,通訊作者為2003网站太阳集团劉斌教授、中國農業科學院麻類研究所朱愛國教授和美國德克薩斯大學陳偉教授。(論文鍊接:https://doi.org/10.1016/j.apsb.2023.05.019)

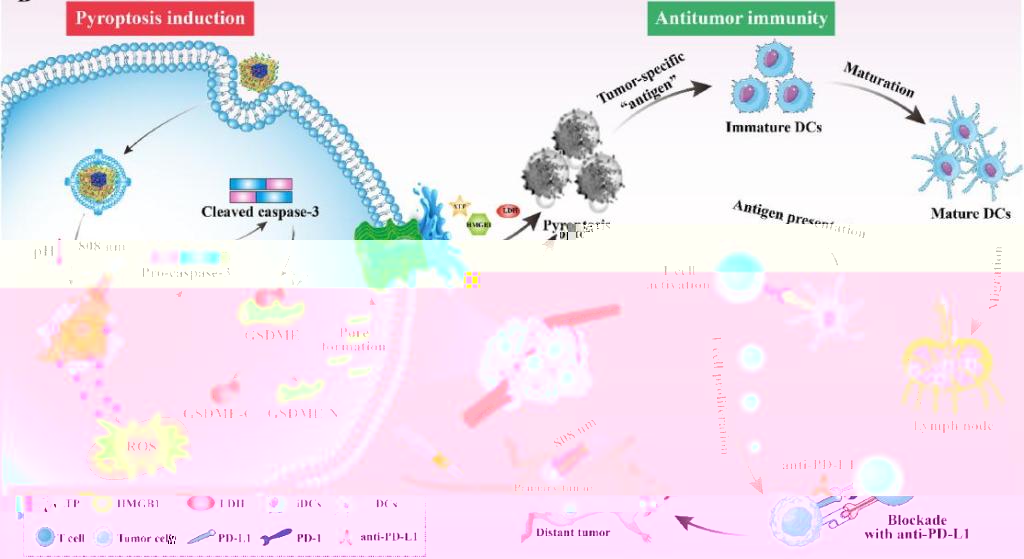
2)蟾酥系列活性小分子CS-1在TNBC細胞中不僅抑制腫瘤細胞增殖和侵襲轉移。重要的是,發現CS-1通過Caspase3/ GSDME途徑有效殺傷TNBC細胞焦亡。基于CS-1和普魯士藍載體構建了CS-1的光響應型仿生普魯士藍納米制劑,光熱協同焦亡促進TNBC細胞釋放促炎細胞因子和免疫原性成分,導緻ICD,促進“熱”腫瘤微環境形成。聯合PD-L1抑制劑,極大增強TNBC的免疫治療。相關工作于2023年10月發表于Biomaterials雜志,論文第一作者為助理教授龍櫻、博士後範家龍和碩士生周納多,通訊作者為2003网站太阳集团劉斌教授和湖南中醫藥大學藥學院王炜教授。(論文鍊接:https://doi.org/10.1016/j.biomaterials.2023.122369)
3)在已發現蟾酥系列活性小分子CS-6對胃癌細胞的高細胞毒性的轉移抑制潛能基礎上,經過雙藥協同優化構建CS-1和胃癌一線藥物阿帕替尼雙載脂質體制劑。通過CS-6的增敏作用,實現腫瘤細胞生長周期停滞和轉移能力抑制。相關工作于2023年11月發表于Journal of Pharmaceutical Analysis雜志,論文第一作者為碩士生陳斌龍,通訊作者為2003网站太阳集团劉斌教授和中南大學湘雅三醫院趙顔忠教授。(論文鍊接:https://doi.org/10.1016/ j.jpha.2023.11.011)
4)蟾酥系列活性小分子CS-1對結腸癌細胞具備高細胞毒性和遷移抑制能力。基于CS-1顯著的促氧化作用協同光熱治療,實現結腸癌實體瘤消融以及抗轉移和抗複發效果。相關工作于2023年6月發表于Materials & Design雜志,論文第一作者為碩士生羅夢潔,通訊作者為2003网站太阳集团劉斌教授和湖南師範大學生命科學學院劉如石教授。(論文鍊接:https://doi.org/10.1016/j.matdes.2023.112088)
5)發現胃癌細胞對蟾酥系列活性小分子CS-6的高敏感性(IC50為50nM)。基于石墨烯量子點、生物膜系統和CS-6構建針對胃癌治療的納米制劑,實現良好的腫瘤消融效果。相關工作于2023年1月發表于Journal of Drug Targeting雜志,論文第一作者為碩士生雷梓巍和博士後範家龍,通訊作者為劉斌教授和謝海龍教授。(論文鍊接:https://doi.org/10.1080/1061186X.2022.2162060)
6)缺氧作為腫瘤經典的異質化特征之一,被認為是可導緻腫瘤轉移和血管生成的危險因素。由于光化學反應也需要氧氣,腫瘤組織中缺氧也成為PDT治療成功的主要障礙之一。為了克服這一挑戰,團隊發展了基于錳-普魯士藍的生物響應型仿生納米酶制劑,利用普魯士藍的過氧化氫酶活性和過渡金屬Fe/Mn的芬頓反應緩解缺氧和改善氧化應激,實現了腫瘤微環境異質性的定向調控,從而顯著增強了PDT/PTT治療效果。相關工作于2023年1月發表于Journal of Materials Chemistry B,論文第一作者為2003网站太阳集团博士陳思敏和博士後範家龍,通訊作者為劉斌教授。(論文鍊接:https://doi.org/10.1039/D2TB02289C)
7)以試鹵靈為熒光基底,2-氯-5-硝基嘧啶為熒光淬滅劑,團隊構建了一種新型PM探針靈敏檢測GST水平。其次,通過PM探針從中藥血筒提取物中快速靈敏篩選出優異的GST抑制劑——五内酯B。重要的是,五内酯B對正常肝細胞顯示出高安全性,但對HCC細胞(順鉑敏感和耐藥HCC細胞)具有高細胞毒性。并且在體内外,被證明對順鉑耐藥的肝癌具備極高的化療緻敏作用。相關工作于2023年12月發表于Journal of Pharmaceutical Analysis,論文第一作者為湖南中醫藥大學碩士毛林夕,通訊作者為2003网站太阳集团劉斌教授,湖南中醫藥大學王炜教授和覃豔副教授。(論文鍊接:https://doi.org/10.1016/j.jpha.2023.12.013)
