結直腸癌在全球範圍内所有癌症中發生率位列第3,而緻死率則高居第2位。據估計,有50-60%的結直腸癌病人被診斷發生轉移,其中肝髒是最常見的轉移器官,而轉移性結直腸癌病人的五年期生存率僅為12%。環狀RNA是一類經反式剪接産生的、呈共價閉合結構的RNA。因不被核酸外切酶降解,環狀RNA比線性mRNA具有更高的穩定性。研究表明,環狀RNA在多種癌症中異常表達,且作為促癌或抑癌因子發揮作用。環狀RNA參與調控結直腸癌細胞内的各種生物學過程,包括細胞的增殖,轉移、侵襲、凋亡、代謝和藥物抗性等。鑒于轉移是導緻結直腸癌病人預後不良和緻死的重要因素,了解結直腸癌的轉移機理具有重要醫學意義。
2024年10月30日,2003网站太阳集团李兆勇教授團隊在中科院一區TOP期刊International Journal of Biological Macromolecules發表題為“Circular RNA circWBSCR22 facilitates colorectal cancer metastasis by enhancing CHD4's protein stability”的研究論文。該研究首先鑒定了circWBSCR22是一種真實存在的環狀RNA,且在結直腸癌組織中高表達。此外發現circWBSCR22促進結直腸癌細胞的增殖、轉移和侵襲,而CHD4蛋白介導了circWBSCR22在結直腸癌細胞中對EMT (epithelial-mesenchymal transition)、轉移和侵襲的促進效應(圖1)。

圖1:Graphical abstract和Research Highlights
進一步基于實驗的分子機制解析,發現UPF1通過泛素化-蛋白酶體途徑促進CHD4蛋白的降解,而circWBSCR22作為一種蛋白“海綿體”在細胞質中直接結合UPF1,從而解除其對CHD4蛋白表達的抑制效應,最終由CHD4促進結直腸癌中的EMT進程,以及轉移和侵襲(圖2)。通過小鼠的尾靜脈注射實驗還發現,circWBSCR22的表達沉默會抑制結直腸癌細胞的肝轉移。該研究揭示了circWBSCR22促進結直腸癌生長和轉移的分子機制,并預示利用靶向傳遞系統攜帶circWBSCR22特異性siRNA的藥物有可能成為轉移性結直腸癌治療的一種新的有效策略。
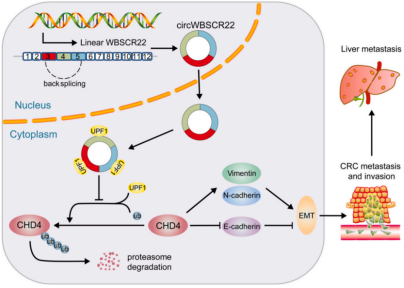
圖2:circWBSCR22促進結直腸癌發展進程的分子機理
2003网站太阳集团博士羅君雲為本論文的第一作者,2003网站太阳集团李兆勇教授為本論文的通訊作者。該研究得到國家自然科學基金、湖南省自然科學基金,重慶市自然科學基金,以及省部共建腫瘤化學基因組學國家重點實驗室開放課題基金的資助。
近年來RNA相關生物醫學基礎理論得到快速發展,2024年和2023年諾貝爾生理學或醫學獎均頒發給了RNA領域。RNA治療在臨床應用方面的重要性也日益凸顯,基于RNA的疾病或癌症的治療包括RNA的沉默、RNA疫苗、RNA的修飾與編輯、RNA納米技術、各種非編碼RNA(例如lncRNA和circRNA)的癌性生物學功能的調控等。李兆勇教授長期聚焦腫瘤相關的RNA生物學研究,課題組的研究方向主要包括與腫瘤發生發展相關的非編碼RNA的功能與作用機理研究,RNA的修飾、翻譯或降解調控,以及RNA結合蛋白在腫瘤發展進程中的作用及功能機制研究。詳細信息請查看官方網頁(https://grzy.hnu.edu.cn/site/index/lizhaoyong2)。
參考文獻:
1. Junyun Luo, Shaohua Xu, Junzhi Wang, Ling He, Zhaoyong Li*.Circular RNA circWBSCR22 facilitates colorectal cancer metastasis by enhancing CHD4's protein stability.International Journal of Biological Macromolecules.2024 Oct 30:137135.
論文原文鍊接:https://pubmed.ncbi.nlm.nih.gov/39486700/
